- ヒト抗体ライブラリー私たちはヒト手術材料由来の扁桃腺、末梢血、骨髄、臍帯血を基に、mRNAを抽出し、RT-PCRによってVH, VLCLを増幅したのち、これをファージミドベクターpTZ19Rに組み込んで7×10^10のレパトアを持つヒト抗体ライブラリAIMSを作製した(文献1)。
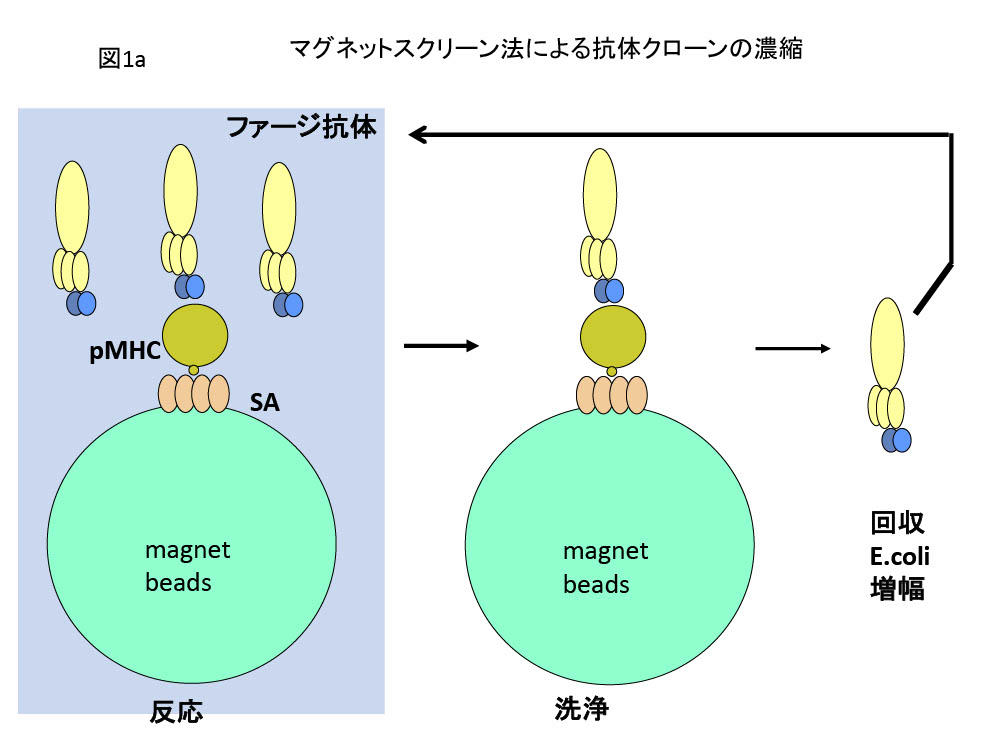
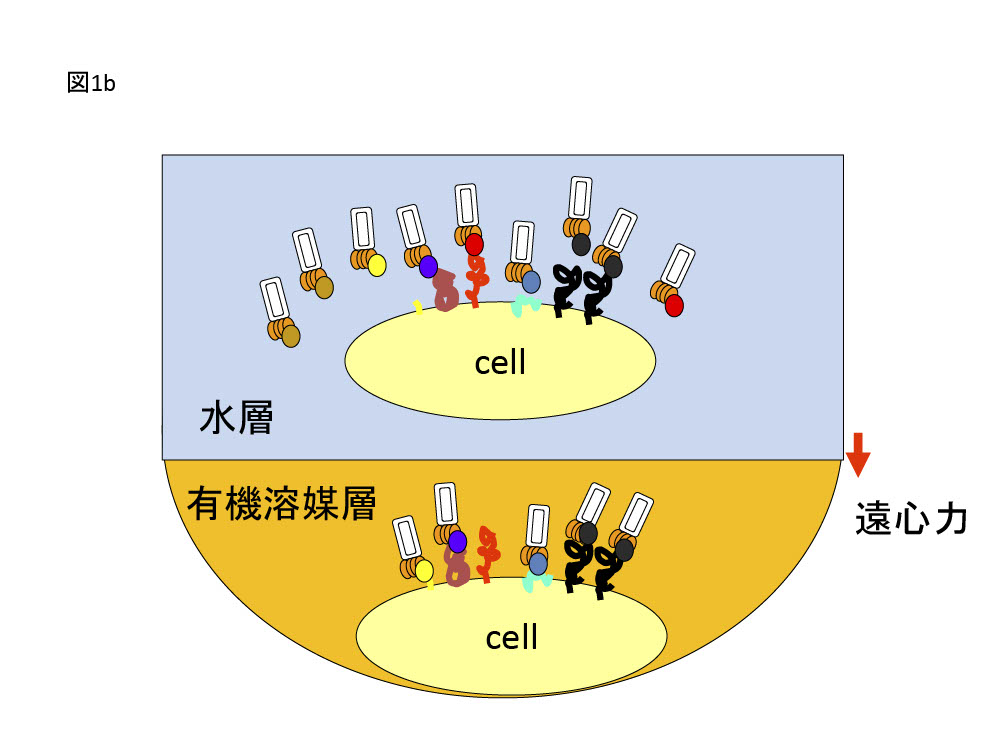
- 抗体スクリーニング ー私たちは、pMHCやさまざまなターゲットタンパクをビオチン化し、これをstreptavidin magnet beadsに結合させたものを1.の抗体ライブラリに反応させたのち洗浄し、大腸菌に感染させて反応性M13phageを得た(図1a)。次にこれをペプチドパルスしたT2細胞または抗原を発現する培養細胞に反応させ、有機溶媒による選択を行ったのち、大腸菌に感染させて反応性M13phageを得た(図1b、文献2)。最後にneutravidinを固相化したplateに希釈したビオチン化抗原を結合させたものを使用したスクリーンを行い結合性の高い抗体を得た。

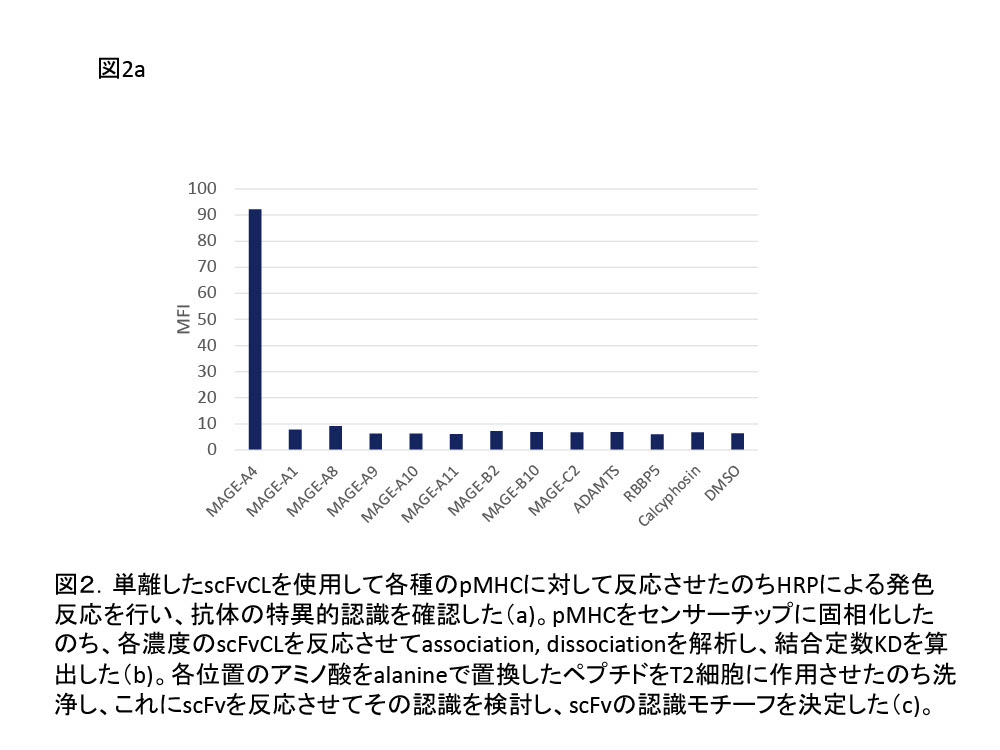
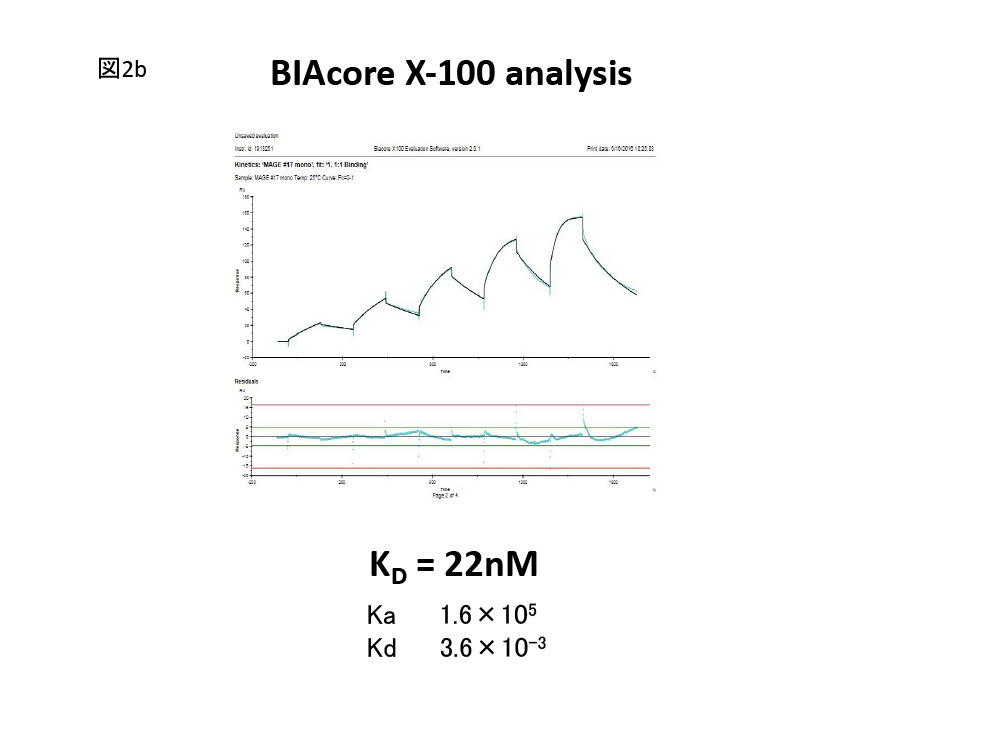
- 抗体評価 ーpMHC認識抗体についての解析は以下のとおりである(文献3)。取得抗体クローンについては配列決定を行って類別した。次にそれぞれのクローンについて各種のpMHCに反応するかどうかをELISAにて検討した(図2a)。次にsurface plasmon resonanse解析により結合定数を決定した(図2b)。さらに、alanineスキャン解析により認識モチーフを決定した(図2c)。タンパク抗原の場合は以下の解析を行った。取得抗体クローンについては配列決定を行って類別した。次にそれぞれのクローンについて各種の抗原発現陽性細胞と陰性細胞についての細胞染色を行い認識特異性の検討を行った。次にsurface plasmon resonanse解析により結合定数を決定した。
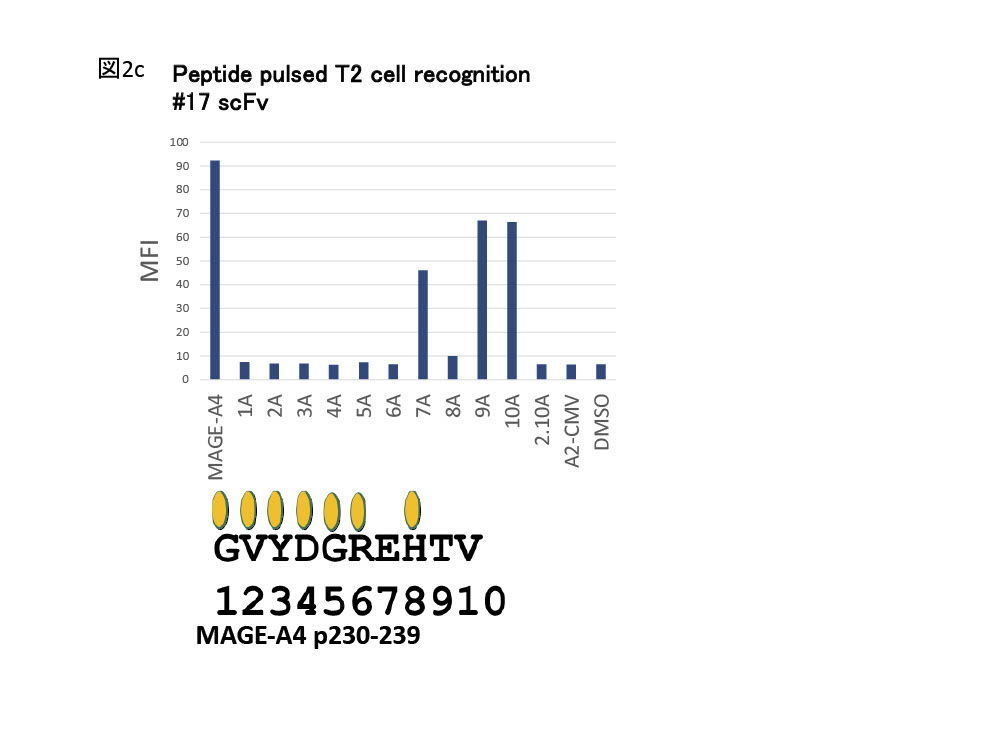
- CARの構築ー取得抗体について、合成オリゴDNAを使用したPCR反応を行ってsignal sequenceを付加したDNA断片を作製し、これを図3に示すレトロウィルス発現ベクターに組み込んだ。
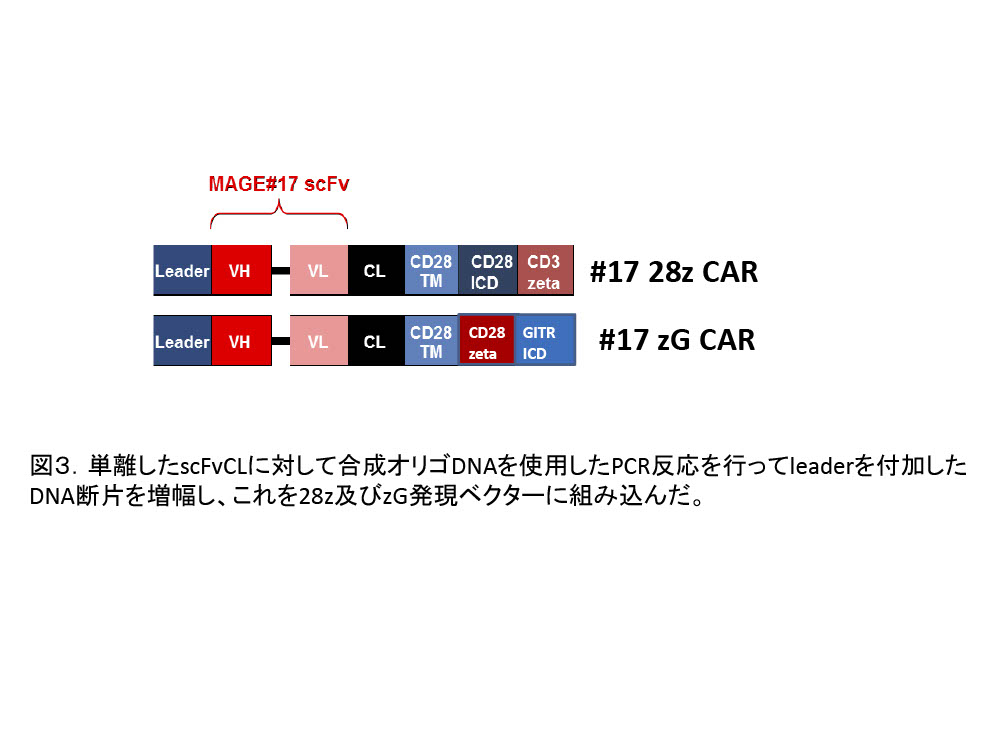
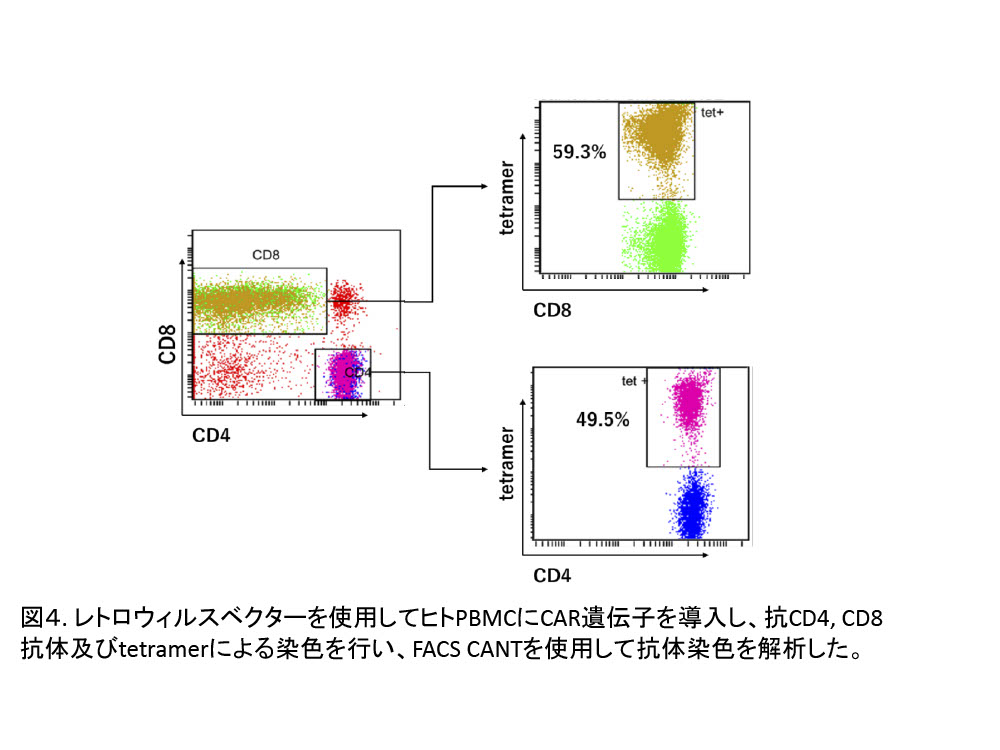
- CAR T細胞の作製ーヒト末梢血T細胞をretronectinとOKT3を使用してプライムし、培養4日後に遠心により固相化したレトロウィルスベクターを感染させてCAR遺伝子の導入を行った。CARの導入効率はtetramer pMHCもしくはビオチン化anti Fab’2を使用した細胞染色によって行う(図4)。 (文責:赤堀)
文献
- Isolation of human monoclonal antibodies that neutralize human rotavirus. Moriguchi, Akahori, Iba, Kurosawa, Taniguchi, J. Virol. 2004, 78(7), 3325-3332
- Isolation of antigen/antibody complexes through organic solvent(ICOS) method. Akahori, Kurosawa G, Sumit2017omo, Morita, Muramatsu, Eguchi, Tanaka, Suzuki, Sugiura, Iba, Sugioka, Kurosawa Y. Biochem. Biophys. Res. Commun. 2009, 378(4) 832-835
- Antitumor activity of CAR-T cells targeting the intracellular oncoprotein WT1 can be enhanced by vaccination. Akahori, Wang, Yoneyama, Seo, Okumura, Miyahara, Amaishi, Okamoto, Mineno, Ikeda, Maki, Fujiwara, Akatsuka, Kato, Shiku, Blood, 2017, 132(11), 1134-1145



 TOP
TOP