CHPナノゲル/蛋白複合体がんワクチン(三重大オリジナルがんワクチン臨床開発)
がんワクチンとして、がん抗原を効率よくリンパ節へ輸送するシステムとして「CHP(Cholesteryl pullulan、コレステリル・プルラン)」を三重大学では独自に開発研究を行ってきました。
2002年に世界で始めてのこのがんワクチンをヒトに投与する臨床試験を開始し、これまでにCHP-HER2ワクチン、CHP-MAGE-A4ワクチン、CHP-NY-ESO-1ワクチンと、3種類の抗原蛋白を利用したがんワクチンの臨床試験を実施しています。
このワクチンのがん治療への有望性が、国の研究事業としても取り上げられ、2004年からは文部科学省がんトランスレーショナル事業に重点課題として選ばれました。CHO-NT-ESO-1がんワクチンの治験が難治食道がんを対象に行なわれて、現在は術後の食道がんを対象にした再発抑制効果を目的として多施設共同治験が全国14機関で行われています。三重大学はその臨床開発の中心であり、様々な基礎研究を展開しています。
これまでのトランスレーショナルリサーチ成果
- CHP-HER2ワクチン first-in-man(ヒトで初めて)のCHPワクチン、安全性と効率よい免疫反応が得られえることがわかりました。 (論文発表Clin Cancer Res. 2006 ;12(24):7397-405.)
- CHP-MAGE-4ワクチン MAGE-A4抗原蛋白を使用したCHPワクチン、安全性と効率よい免疫反応が得られえることがわかりました。三重大学、北海道大学、大阪大学、北野病院(大阪市)、産業医科大学、長崎大学との共同研究。 (論文発表 Immunotherapy. 2016;8(5):527-40,Vaccine. 2014 ;32(45) :5901-7)
- CHP-NY-ESO-1ワクチン NY-ESO-1抗原蛋白を使用したCHPワクチン。治験として医薬品医療機器総合機構(PMDA)へ届けをだした初めての臨床第Ⅰ相試験。安全性とワクチン蛋白の用量に応じた免疫反応性と生存延長があることがわかりました。(論文発表 J Transl Med. 2013 Oct 5;11:246)
- CHP-NY-ESO-1ワクチン/CHP-HER2ワクチン・アジュバントOK-432 2種のワクチンとOK-432を免疫賦活剤として使用する混合ワクチン。2つの抗原に対してが同時に免疫反応が起こされることがわかりました。OK-432への免疫反応は起こらないこともわかりました。(論文発表Vaccine. 2009 ;27(49):6854-61)
実施中のCHPワクチン臨床試験
- CHP-NY-ESO-1/MIS416 NY-ESO-1ワクチンの効果を高めるために免疫賦活剤としてMIS416(ニュージーランド製)を同時し投与するワクチン。MIS416はアクネ(にきび)菌由来の成分でToll-like受容体を刺激する(自然免疫活性化)ものです。現在、試験参加者募集中。
- CHP-NY-ESO-1/Poly;IC:LC NY-ESO-1ワクチンの効果を高めるために免疫賦活剤としてPoly;IC:LC(アメリカ製)を同時し投与するワクチン。Poly;IC-LCは短いDNA配列でToll-like受容体を刺激する(自然免疫活性化)ものです。現在、試験参加者募集中。臨床試験は京都府立医科大学(消化器内科)で実施されています。
- CHP-NY-ESO-1(早期第Ⅱ相医師主導治験) 食道がんは約30%の例でNY-ESO-1抗原が、がん細胞に発現されています。抗がん剤、手術を終了した食道がんを対象にCHP-NY-ESO-1ワクチンを投与し、再発抑制効果があるかどうかを調べる臨床試験です。54例の登録が終了し、現在結果をみているところです。
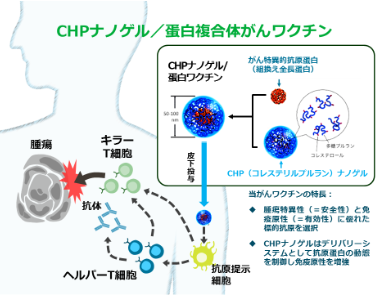
CHPナノゲル/蛋白複合体がんワクチンの原理
がん抗原として現在最も臨床は開発が進んでいる「NY-ESO-1」を例にとります。医薬品として使用でききるように、人工的に蛋白質を合成します。遺伝子組み換え技術を使って、大腸菌を使って合成します。もう一つの材料として、コレステリル・プルラン(疎水化多糖、糖の一種、CHPと呼びます)を人工合成します。これらの二つを水溶液中で混和させると、NY-ESO-1蛋白分子がCHPの中に取り込ませた複合体が自然凝集します。これをがんワクチン製剤とするものです。
これまでの三重大学での基礎研究(動物実験、ヒト細胞のin vitro実験)で、CHPワクチンはがん抗原に特異的なキラーT細胞とヘルパーT細胞の両方を活性化することを明らかにしてきました。この技術は特許として申請されています。



 TOP
TOP